2024年欧洲肿瘤内科学会(ESMO)年会于当地时间9月13日至17日在西班牙巴塞罗那以线上+线下形式召开。中山大学附属肿瘤医院王树森教授在会上口头报告了贝达药业泰瑞西利联合氟维司群治疗既往内分泌治疗后进展的HR+/HER2-晚期乳腺癌III期临床研究(Tiffany)期中分析结果。
研究数据
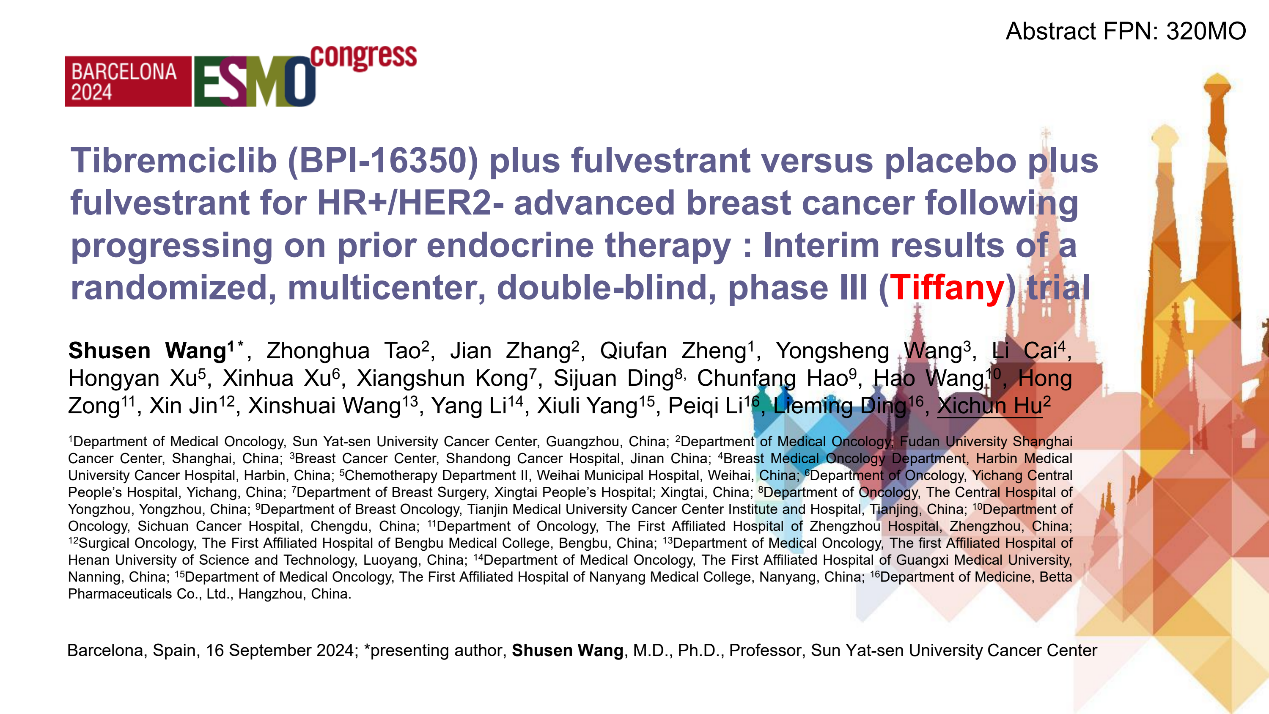
Tiffany研究是一项多中心、随机、双盲、平行对照的Ⅲ期临床研究。研究共纳入274名患者(既往接受内分泌治疗后进展的HR+/HER2-局部晚期、复发或转移性乳腺癌受试者),按2:1随机分组到泰瑞西利联合氟维司群组(n=184)或安慰剂联合氟维司群组(n=90)。泰瑞西利联合氟维司群组患者每天口服400 mg泰瑞西利,肌肉注射500 mg氟维司群(第一周期D1和D15各给药一次,后续每周期给药一次),安慰剂联合氟维司群组患者每天口服400 mg安慰剂,肌肉注射500 mg氟维司群(第一周期D1和D15各给药一次,后续每周期给药一次)。每个给药周期为28天,用药直至患者出现疾病进展、满足退出标准或研究终止标准。
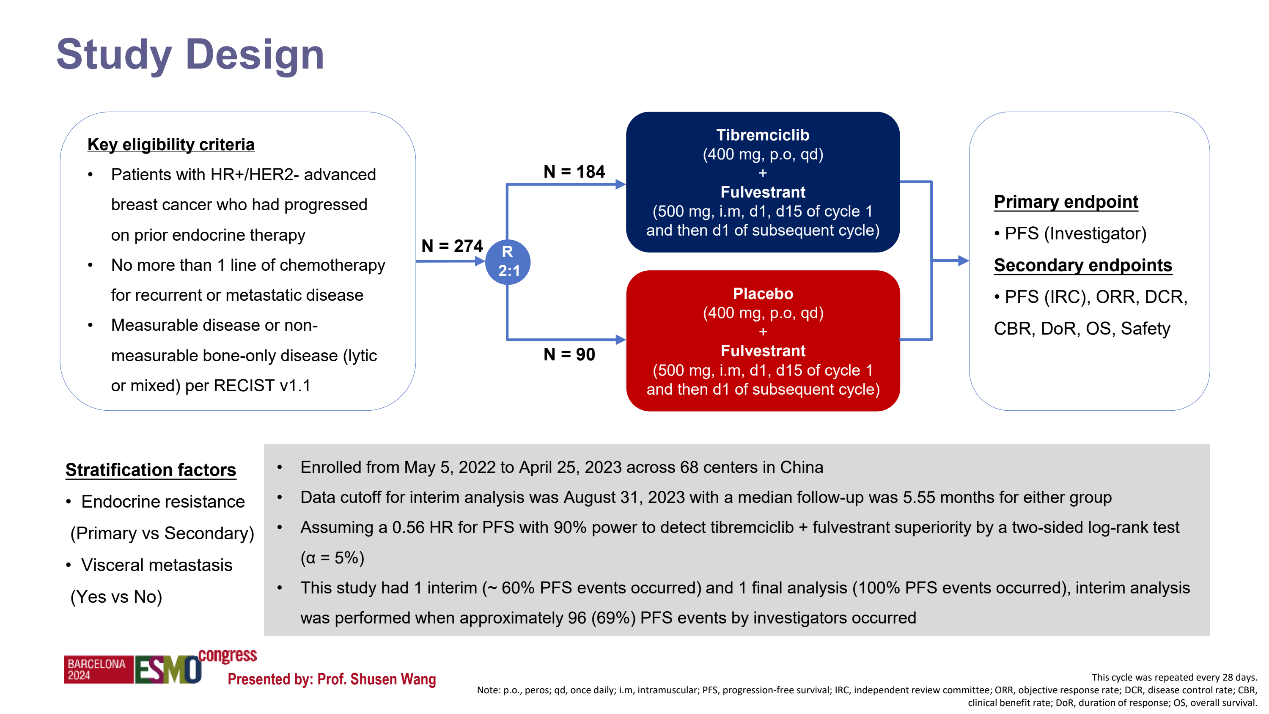
本研究主要疗效终点为研究者评估的PFS。截至2023年8月31日的数据显示,研究者评估的泰瑞西利联合氟维司群组和安慰剂联合氟维司群组的中位PFS分别为11.1个月(95%CI 9.2–12.8)和5.5个月(95%CI 4.2–7.4)。与安慰剂联合氟维司群治疗相比,泰瑞西利联合氟维司群治疗能够显著改善PFS,将患者疾病进展或死亡的风险降低了69%(HR 0.31; 95%CI 0.21–0.47; P<0.0001)。IRC评估的PFS与研究者评估的结果一致(HR 0.31; 95%CI 0.19–0.48; P<0.0001)。
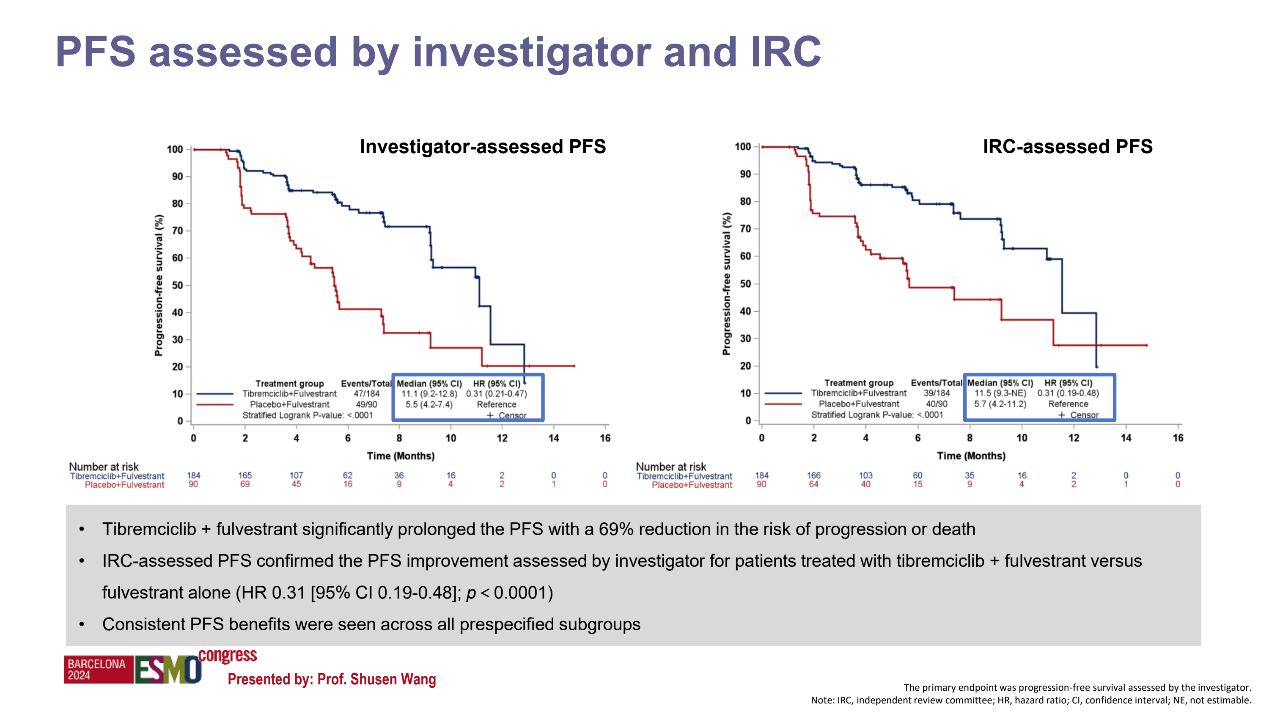
泰瑞西利联合氟维司群用于既往内分泌治疗后进展的HR+/HER2-晚期乳腺癌患者显示出良好的耐受性,TEAE(不良事件)多为轻至中度,常见不良反应包括腹泻、中性粒细胞减少、白细胞减少等。可见,泰瑞西利联合氟维司群用于既往内分泌治疗后进展的HR+/HER2-晚期乳腺癌患者的临床获益优于安慰剂联合氟维司群组,且整体耐受性良好。
泰瑞西利III期主要研究者、复旦大学附属肿瘤医院肿瘤内科主任胡夕春教授表示,泰瑞西利III期临床研究数据的公布,可为内分泌治疗耐药的HR+/HER2-转移性晚期乳腺癌患者提供新的治疗选择。期待国产泰瑞西利能够早日上市,为中国患者带来福祉的同时,向世界贡献出更多有益的“中国方案”。
泰瑞西利III期主要研究者、中山大学附属肿瘤医院内科乳腺病区主任王树森教授表示,CDK4/6抑制剂联合内分泌治疗已成为国际和国内指南推荐的标准方案。泰瑞西利III期临床研究期中分析数据的公布,意味着更多内分泌治疗耐药的HR+/HER2-晚期乳腺癌患者将能从规范治疗中获益。期待泰瑞西利早日上市,为临床医生和患者提供全新的治疗选择。
贝达药业副总裁李培麒表示,泰瑞西利是中国自主研发的CDK4/6抑制剂,主要用于治疗HR+/HER2-晚期或转移乳腺癌患者。截至目前,I期、III期研究结果均显示在内分泌治疗后进展的HR+/HER2-晚期乳腺癌中,泰瑞西利联合氟维司群均表现出了积极的治疗反应和良好的耐受性。目前该药已提交NDA,期待能早日获批,为患者的治疗提供更多更优的选择方案。
关于泰瑞西利
泰瑞西利是贝达药业自主研发的具有全新结构的细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂。在激酶水平上,泰瑞西利在CDK家族中展示出了良好的CDK4/6靶点选择性,对CDK4/6的抑制活性与已获批上市的同靶点产品相当。在I期研究中泰瑞西利单药治疗或与氟维司群联合治疗均对晚期乳腺癌患者表现出良好的耐受性和初步的抗肿瘤活性。本次研究是一项多中心、随机、双盲、平行对照的III期临床试验,纳入患者为既往接受内分泌治疗后进展的HR+/HER2-局部晚期或晚期复发转移性乳腺癌患者。本研究结果表明泰瑞西利联合氟维司群表现出了积极的治疗反应和良好的耐受性,目前该药已提交NDA。
关于CDK4/6
CDK4/6是一类丝氨酸/苏氨酸激酶,与细胞周期因子D结合,催化抑癌基因Rb的磷酸化,从而调节细胞由G1期向S期转换。CDK4/6抑制剂被证明是对抗内分泌耐药后进展的有效治疗药物,能够高效精准地抑制乳腺癌细胞中CDK4/6激酶的活性,阻断Rb蛋白磷酸化,从而阻滞细胞周期从G1期到S期的进程,进而抑制肿瘤细胞增殖;同时,CDK4/6抑制剂抑制上游雌激素受体信号通路的表达,与内分泌治疗之间存在协同增效的作用,达到延缓和逆转内分泌耐药。目前,我国已有哌柏西利、瑞波西利、阿贝西利和达尔西利4款CDK4/6抑制剂获批上市,但国内接受内分泌治疗后疾病进展的HR+/HER2-晚期或转移性乳腺癌的治疗需求远未得到满足,国产原研药物的研发上市有望给中国乳腺癌患者带来更多治疗选择。
下一条: 新进展!禾元生物植物源重组人血清白蛋白注射液上市申请获受理并纳入优先审评
