
4月17日-22日,2026年第117届美国癌症研究协会(AACR)年会在美国加利福尼亚州圣地亚哥举行。贝达药业自主研发的新型口服泛RAS(ON)抑制剂BPI-572270首次人体I/II期临床研究方案入选本次会议。本研究的主要研究者为浙江省肿瘤医院宋正波教授。
△AACR年会现场

△贝达团队参加AACR年会
01 研究背景
KRAS突变是多种肿瘤类型(包括胰腺癌、结直肠癌和非小细胞肺癌)中最常见的致癌驱动因素之一。尽管KRAS G12C抑制剂已获得监管批准,但针对其他非G12C KRAS突变(如G12D、G12V、G12R)的有效疗法仍存在迫切未满足的临床需求。
BPI-572270是一种新型、口服、亲环蛋白A(Cyclophilin A)依赖性泛RAS(ON)抑制剂,可选择性地靶向GTP结合状态的RAS蛋白。通过与亲环蛋白A和活化RAS蛋白形成三复合物,BPI-572270阻断RAS(ON)与下游效应蛋白之间的相互作用,从而抑制致癌RAS信号通路和肿瘤生长。

△BPI-572270分子作用机理图
02 临床前活性
在临床前模型中,BPI-572270展现了显著的抗肿瘤活性:在不同KRAS、NRAS和HRAS突变细胞系中表现出强效的肿瘤细胞增殖抑制活性(亚纳摩尔级IC50);在多种KRAS突变的小鼠模型中,口服BPI-572270(0.3-3 mg/kg/天)可显著抑制肿瘤生长甚至使肿瘤消退。
03 临床研究方法
本研究是一项首次人体、开放标签、多中心I/II期临床研究,评估BPI-572270单药治疗RAS突变晚期实体瘤患者。
研究包含三个部分:A部分(剂量递增):采用回填贝叶斯最优区间(BF-BOIN)设计,BPI-572270每日口服一次,剂量从1 mg/天递增至20 mg/天,评估安全性、药代动力学,并确定最大耐受剂量(MTD),21天窗口期评估剂量限制性毒性(DLT)。B部分(剂量扩展):进一步评估A部分选定剂量的安全性、药代动力学和初步抗肿瘤活性,确定II期推荐剂量(RP2D)。扩展队列将纳入RAS突变晚期癌症患者,包括胰腺癌、非小细胞肺癌、结直肠癌等。C部分(II期试验):患者以RP2D入组扩展队列,根据RECIST v1.1标准进一步评估抗肿瘤疗效。
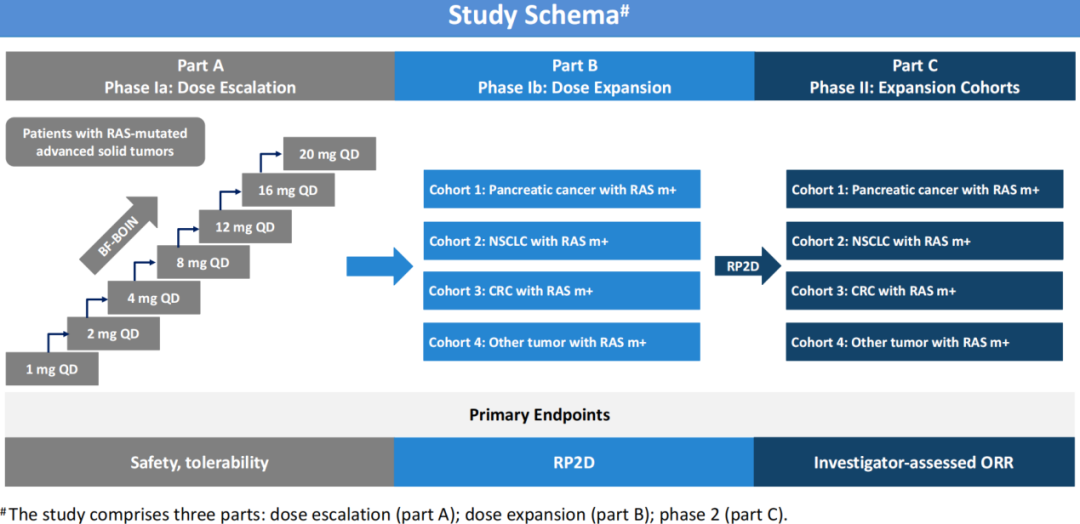
△BPI-572270胶囊I/II期临床研究方案示意图
关键入排标准为:年龄≥18岁;经组织学确认的转移性或局部晚期实体瘤;标准治疗后进展或不耐受/不符合标准治疗条件;确认RAS突变状态;既往未接受过KRAS G12C或其他RAS抑制剂治疗(剂量递增阶段除外);ECOG PS评分≤1;器官功能良好。
04 临床试验进展
BPI-572270胶囊I/II期临床研究已正式启动,临床试验ClinicalTrials.gov注册号为NCT07435038。I期临床研究首例患者已于2026年1月29日入组。
05 结论
临床前数据显示,BPI-572270在多种RAS突变肿瘤模型中具有强效抗肿瘤活性。正在进行的I/II期临床研究将进一步评估BPI-572270胶囊在RAS突变晚期实体瘤患者中的安全性、药代动力学和初步疗效。
下一条: 贝达药业控股子公司Xcovery与美国Eversana公司达成恩沙替尼商业化合作
