新闻中心 / News Center
贝达药业CD73小分子抑制剂BPI-472372获批开展临床试验
日期: 2023-03-14
近日,贝达药业收到国家药品监督管理局签发的《药物临床试验批准通知书》(通知书编号:2023LP00307、2023LP00308),公司申报的CD73小分子抑制剂BPI-472372片拟用于晚期实体瘤的临床试验申请已获国家药品监督管理局批准开展。
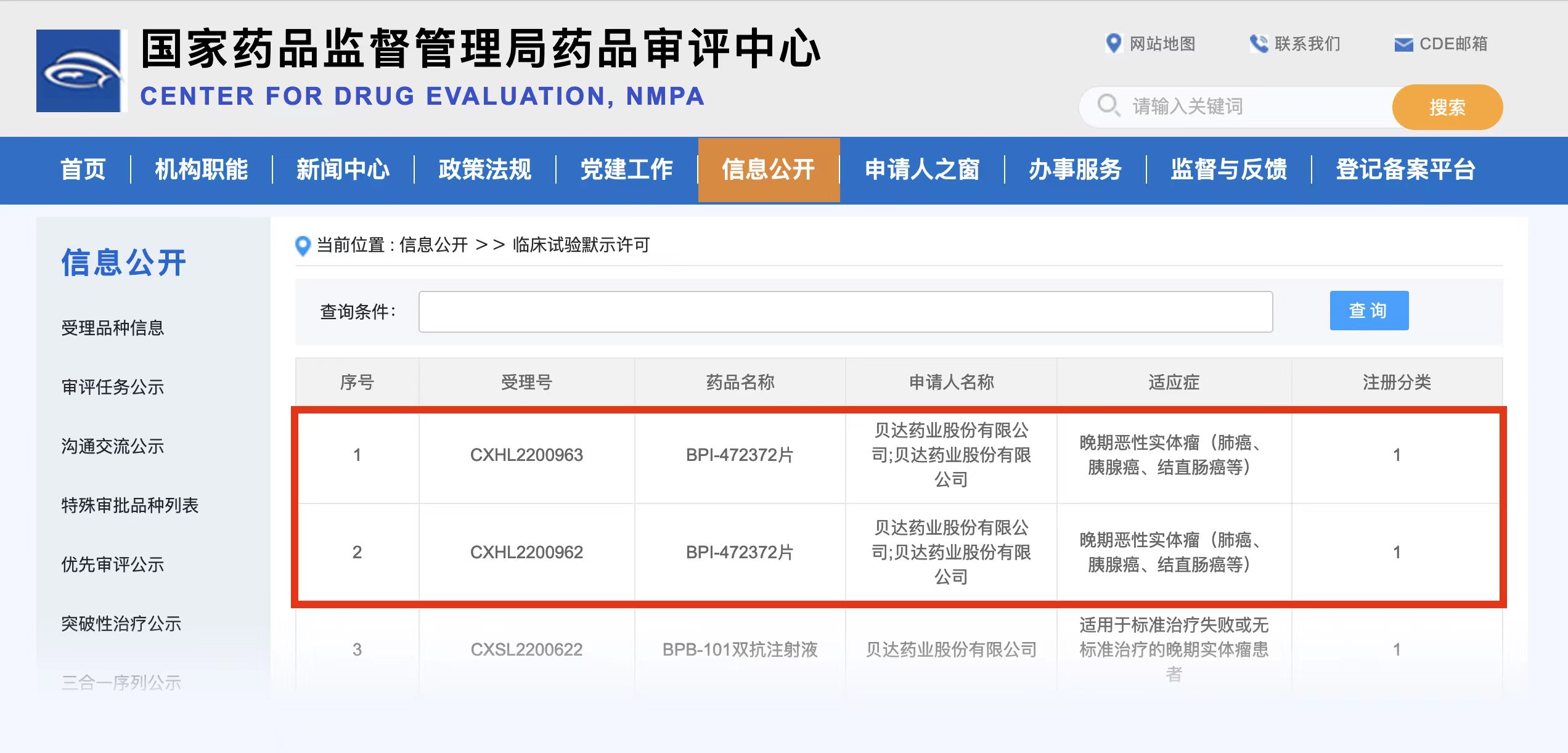
BPI-472372是由贝达药业自主研发的拥有完全自主知识产权的新分子实体化合物,属于高效、特异性CD73口服小分子抑制剂。
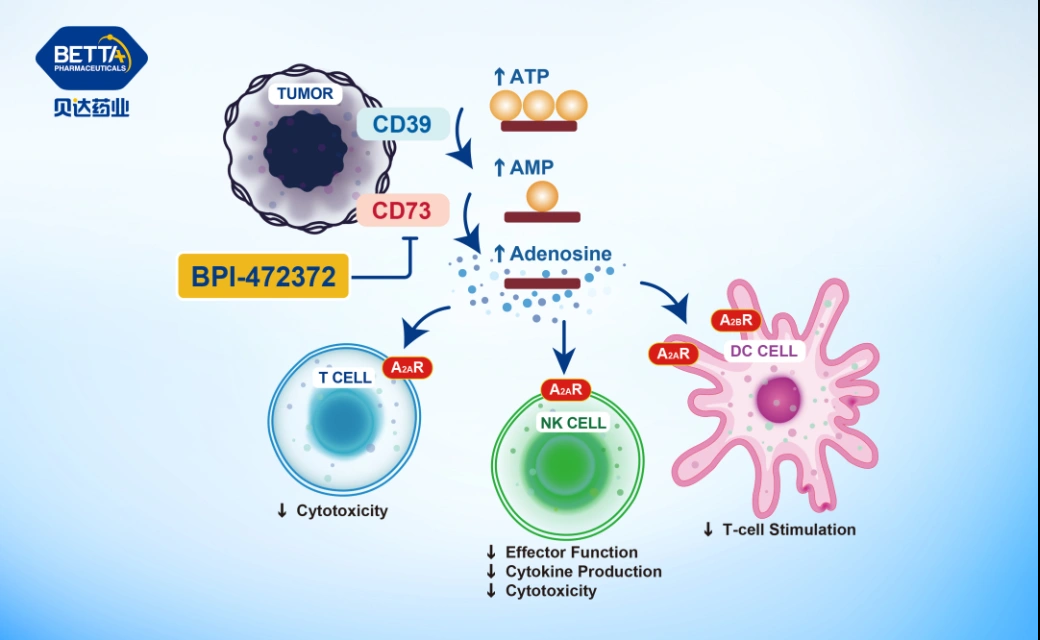
△BPI-472372作用机理图
临床前研究显示,BPI-472372能够特异性抑制CD73核苷酶的活性,下调肿瘤微环境中腺苷的水平,通过解除肿瘤免疫抑制从而发挥抗肿瘤作用。BPI-472372临床前研究展现出优秀的体外及体内活性、药代动力学性质及良好的安全性。
贝达药业杭州研发中心主任吴颢博士表示,作为代谢免疫检查点,CD73-腺苷代谢通路的异常激活参与肿瘤免疫逃逸、促进肿瘤的生长和转移,并与患者预后不良相关。此次BPI-472372获批临床,是对贝达肿瘤免疫研发管线的补充和扩展。BPI-472372有望通过单药或联合疗法应用于非小细胞肺癌、胰腺癌等晚期实体瘤患者,具有广阔的应用前景。
贝达药业资深副总裁兼首席科学家王家炳博士表示,相较于抗体,小分子药物分子量较小,可有效避免大分子药物引发的免疫原性问题。CD73小分子抑制剂BPI-472372具有优秀的口服生物利用度、更好的组织渗透性,未来可作为单一疗法或与抗体药、传统化疗药相结合,进一步提高肿瘤疗效或改善免疫检查点抑制剂耐药问题。期待本品能够早日获批上市,惠及患者。
下一条: 踏上新征程 奋楫再出发| 丁列明委员传达全国两会精神
热门点击
